В январе 2026 сразу несколько научных групп из Китая представили результаты по медицинским нанороботам, которые нацелены на лечение без традиционной хирургии. Речь идет о трех направлениях, где цена точности особенно высока: онкология, тромбы и аневризмы головного мозга. Это не готовые процедуры для клиник, но уже и не чистая фантазия. В работах появляются конкретные механизмы движения, навигации и доставки препарата, а результаты на животных моделях становятся измеримыми.
Самый громкий кейс пришел из Уханьского технологического университета. Ученые описали инъекционных нанороботов для точечной терапии опухолей. Основа системы - наночастицы золота и два фермента. Уреаза использует эндогенную мочевину в крови и микроокружении опухоли как источник движения, а каталаза помогает ориентироваться по градиенту перекиси водорода, который характерен для опухолевых тканей. Работа опубликована в National Science Review и выглядит как прямой ответ на вопрос, который журнал Science формулировал еще в 2021 году: станут ли инъекционные нанороботы реальностью.
Цифры в их экспериментах на мышах с опухолями впечатляют даже по меркам доклиники. Нанороботы накапливались в опухоли в 209 раз эффективнее пассивной диффузии, проникали в ткань более чем в 10 раз глубже, а интернализация в клетки была выше в 1970 раз. Если их нагружали противоопухолевым препаратом, эффективность подавления опухоли возрастала примерно в 49 раз по сравнению с пассивными аналогами. Команда сообщает, что создала компанию, которая занимается продвижением этой технологии к медицинскому применению, и рассчитывает, что при дальнейшей оптимизации система сможет перейти от экспериментальных моделей к клинической практике.
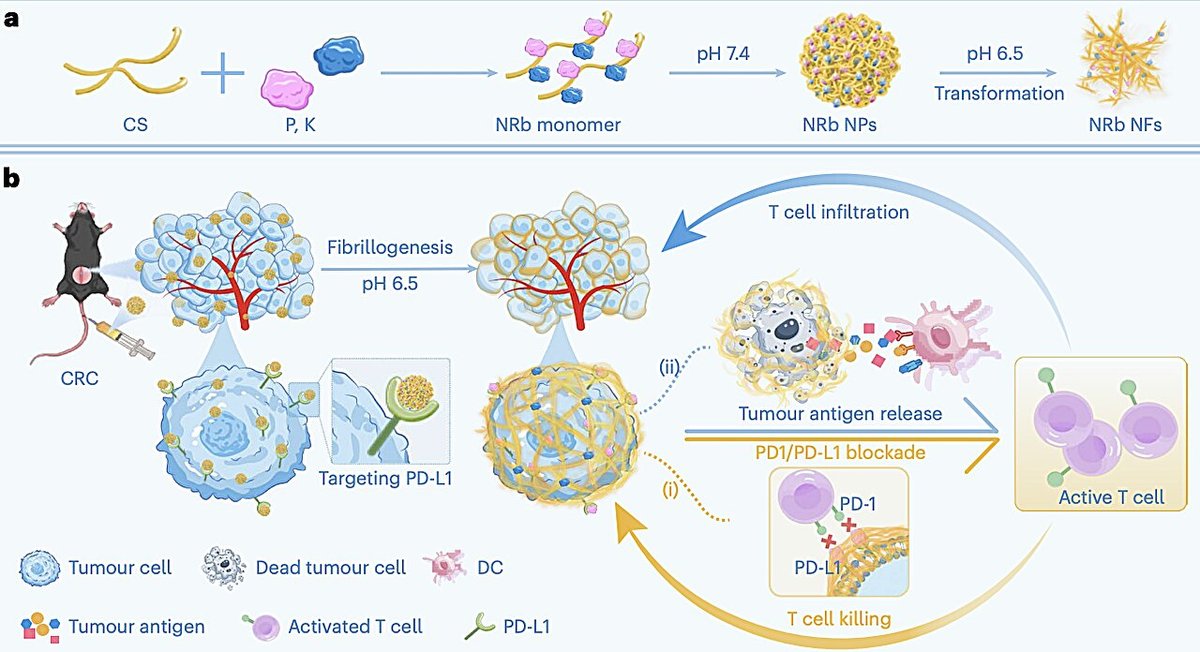
18 января 2026 другой консорциум китайских исследователей, в том числе из Армейского медицинского университета (госпиталь Синьцяо) и Центра передового опыта по нанонауке Китайской академии наук, представил нанороботов для иммунотерапии колоректального рака. Здесь идея другая: робот это специально сконструированная пептидная последовательность, которая распознает белок PD-L1 на клетках опухоли. По заявлению авторов, система дала более высокую терапевтическую эффективность по сравнению с комбинацией антител к PD-L1 и оксалиплатина в разных моделях опухолей у мышей, а также показала хорошую биосовместимость благодаря целевому разрушению раковых клеток.
Тромбы и аневризмы: когда важны минуты и миллиметры
Нанороботы для тромболизиса показали в марте 2025 исследователи из Харбинского медицинского университета и Харбинского политехнического университета. Профессор Лэн Сяопин объяснял, почему классическая терапия иногда работает медленно: при ламинарном кровотоке препарату трудно проникнуть в центр тромба. Предложенная технология помогает нанороботам пройти через слои такого потока и ускорить доставку лекарства.
Инженерная часть вдохновлена механизмом движения кишечной палочки E. coli. Она вращает жгутики и создает микровихри. Исследователи воспроизвели этот механизм и собрали самоорганизующиеся нанороботы с направленным вращением. Во вращающемся магнитном поле они формируют лекарственные вихри и точнее нацеливаются на тромб. В экспериментах на животных с моделью тромбоза нижней полой вены у крыс, где кровоток контролировали допплеровским ультразвуком, система очистила тромб размером 4 мм за 6 минут. Также отмечается преимущество при удалении старых плотных тромбов. В течение 14 дней устройства могли естественно деградировать, не вызывая инвазивности, боли и токсичных побочных эффектов.
Отдельная линия это аневризмы мозга. Международная команда из Эдинбургского университета и Шестой народной больницы Шанхая разработала магнитных нанороботов, которые доставляют белок для свертывания крови внутри аневризмы. Речь идет о миллиардах микророботов диаметром около 300 нанометров, это примерно одна двадцатая ширины человеческого эритроцита. Лекарство находится в защитной оболочке, которая плавится при определенной температуре.
После введения нескольких сотен миллиардов таких устройств в артерию кролика исследователи с помощью магнитов и медицинской визуализации заставляли нанороботов собираться внутри аневризмы. Затем внешние магнитные источники нагревали их до точки плавления оболочки, и высвобождался белок, который блокировал аневризму и предотвращал или останавливал кровотечение в мозг. Результаты были показаны на лабораторных моделях и на небольшом количестве кроликов, проверка через две недели подтверждала эффект. Исследование опубликовано в Small в сентябре 2024 года. Руководитель работы доктор Ци Чжоу из Эдинбургской школы инженерии отмечал, что такие системы открывают путь к ремонту сосудов с меньшими рисками и доставке лекарства с точностью до миллиметра в труднодоступные зоны.
Информация
Авторы указывают, что метод может улучшить существующие техники, где врачи проводят микрокатетер по сосудистой сети и вводят устройства для остановки или перенаправления кровотока.
Новая идея потенциально снижает риск отторжения имплантируемых материалов и уменьшает зависимость от антитромботических препаратов, которые способны вызывать кровотечения и проблемы с желудком. Плюс отпадает необходимость вручную формировать микрокатетер для сложной навигации по мелким сосудам, задача, которая иногда занимает часы.
Где граница между прорывом и процедурой
В 2025 российские ученые опубликовали этический кодекс для медицинских изделий на базе наноробототехники. Среди принципов фигурируют приоритет биосовместимости материалов на молекулярном и системном уровнях, контроль таргетирования и предсказуемости жизненного цикла устройств, приоритет благополучия пациента над коммерческими интересами, запрет на автономное принятие решений устройствами и ограничение репликации.
На пути к клинике остаются тяжелые вопросы. Это токсичность и биосовместимость некоторых наночастиц, масштабирование производства от лаборатории к промышленному выпуску, регуляторные требования и необходимость длительных испытаний. Нужно понимать, как частицы взаимодействуют с организмом, как выводятся и какие долгосрочные эффекты могут появляться. Поэтому приоритетом называют разработку биосовместимых и биоразлагаемых материалов.
Рынок при этом растет. Мировой рынок систем доставки лекарств на основе нанотехнологий в 2025 году оценивался в $107,65 млрд и, по прогнозам, может превысить $261,95 млрд к 2037 году. Российский рынок медтехнологий тоже ускоряется: за три квартала 2025 он вырос на 80,1% по сравнению с тем же периодом 2024 года, а выручка 75 российских MedTech-компаний в третьем квартале 2025 составила 16,2 млрд рублей. Прогноз на 2030 год предполагает рост объема рынка медтеха с 1 трлн рублей в 2024 до 2,3 трлн рублей.
Нанороботы действительно находятся на переднем крае биомедицины, и результаты на животных моделях становятся все более предметными. Но путь к реальной клинической практике зависит от того, насколько быстро исследователи решат вопросы безопасности, контроля и масштабируемости, а регуляторы смогут оценить риски и допустить технологию до людей. Пока это научные прорывы, а не процедура, которую можно завтра увидеть в обычной больнице.
Есть новость? Станьте автором.
Мы сотрудничаем с независимыми исследователями и специалистами по кибербезопасности. Отправьте нам новость или предложите статью на рассмотрение редакции.




